Pri meraní sme nevzali do úvahy tepelnú kapacitu kalorimetra. Toto meranie bolo realizované na hodine fyziky 7.B v roku 2024.
- Prázdny kalorimeter sme položili na digitálnu váhu, stlačili sme tlačítko Tara
- Do kalorimetra sme naliali studenú vodu a digitálna váha odmerala jej hmotnosť.
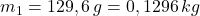
- Do kalorimetra sme vložili teplomer, počkali sme, kým sa teplota ustáli.
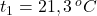
- V rýchlovarnej kanvici sme zohriali vodu, do kadičky sme vložili železnú kocku a zaliali ju horúcou vodou. Po niekoľkých minútach sme odmerali teplotu vody v kadičke, túto teplotu sme pokladali za teplotu kocky.
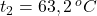
- Kocku sme rýchlo vybrali z kadičky a vložili do kalorimetra.
- Čakali sme, kým teplota vody v kalorimetri stúpala, keď prestala stúpať, zapísali sme dosiahnutú teplotu.
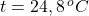
- Vypočítali sme množstvo tepla, ktoré kocka odovzdala vode
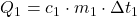
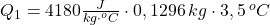
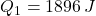
- Množstvo prijatého a odovzdaného tepla je rovnaké.
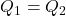
- Odovzdané teplo možno vyjadriť ako súčin tepelnej kapacity kocky a rozdielu pôvodnej a konečnej teploty.
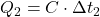

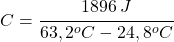
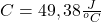
- Hmotnostnú tepelnú kapacitu dostaneme ako podiel tepelnej kapacity telesa a jeho hmotnosti. Odvážili sme hmotnosť železnej kocky a vypočítali sme hmotnostnú tepelnú kapacitu železa.
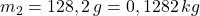
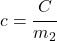

- Vo fyzikálno-chemických tabuľkách sme vyhľadali hmotnostnú tepelnú kapacitu železa, jej hodnota je:
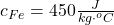
Nami nameraná hodnota bola o 14,44% menšia než tabuľková.
Analýza prečo sme namerali menej, než je v tabuľkách?
- Nevzali sme do úvah tepelnú kapacitu kalorimetra. Kocka odovzdala teplo nielen vode, ale aj kalorimetru. Keď ju odmeriame, môžeme naše meranie upresniť.
- Vždy sa dopúšťame nejakej chyby merania, pri meraní teploty sme sa mohli pomýliť trikrát najmenej o pol desatiny stupňa, chyby sme sa mohli dopustiť aj pri meraní hmotnosti vody a kocky.
- Pri pokuse dochádzalo aj k tepelnej výmene s prostredím, pri prenose kocky do kalorimetra a hoci je kalorimeter zostrojený tak, aby sa minimalizovala tepelná výmena s okolím, predsa len k nejakej výmene dochádza.
Vzhľadom na vyššie uvedené je 14,44% chyba prijateľná.